Die Hämochromatose ist eine Eisenspeicherkrankheit. Unbehandelt führt sie zu schwerwiegenden Organstörungen, wie einer Leberzirrhose, einer Zuckerkrankheit, Gelenkschäden und einer Herzkrankheit mit lebensbedrohlichen Rhythmusstörungen. 1 2 3
Das Wichtigste verständlich
| Kurzgefasst |
| Die Hämochromatose ist eine Erkrankung, bei der der Körper Eisen unkontrolliert aufnimmt und im Übermaß in verschiedenen Organen und Geweben speichert. Der Körper hat keinen Mechanismus, Eisen kontrolliert wieder auszuscheiden. Die Eisenspeicherung im Herzen, in der Leber, in der Bauchspeicheldrüse oder in den Gelenken führt zu einer vielfältigen Symptomatik. Wird die Erkrankung frühzeitig erkannt, kann eine wirkungsvolle Therapie eingeleitet und diesen Komplikationen vorgebeugt werden. Eine genetische Untersuchung naher Blutsverwandter gehört zur Vorsorge.
Befallene Organe
Diagnosestellung: Die Erkrankung wird meist im Alter von 40-50 Jahren diagnostiziert, bei Frauen wegen der Monatsblutungen etwas später als bei Männern. Hohe Erythrozytenzahlen (viele rote Blutkörperchen), ein erhöhtes Serum-Ferritin und eine hohe Transferrinsättigung weisen auf die Diagnose. Eine Genanalyse kann sie bestätigen und dient auch der vorbeugenden Familienuntersuchung. Die wirksamste Therapie besteht in Aderlässen unter ständigen Kontrollen des Blutbilds und des Eisenspiegels im Blut. Wenn Aderlässe wegen einer zu ausgeprägten Blutarmut (Anämie) nicht durchgeführt werden können, kommen Medikamente in Betracht, die Eisen binden und ausscheidungsfähig machen. Das gebräuchlichste ist Desferrioxamin. Im Endstadium einer Leberzirrhose und bei frühzeitig erkanntem Leberkrebs kommt eine Lebertransplantation in Betracht. Sie führt jedoch nicht zu einer Heilung, da der eigentliche Grund für die Eisenüberladung in einer unkontrollierten Eisenaufnahme im Darm liegt. → Hämochromatose – einfach erklärt |
→ Auf facebook informieren wir Sie über Neues und Interessantes.
→ Verwalten Sie Ihre Laborwerte mit der Labor-App Blutwerte PRO – mit Lexikonfunktion.
Definition
Die Hämochromatose ist eine Speicherkrankheit, die zu ausgeprägten Eisenablagerungen in verschiedenen Organen, besonders in der Leber, führt (> 0,5 µg/100 g Feuchtgewicht, > 700 µg/g Trockengewicht). Bei Eisenablagerungen unterhalb dieses Wertes spricht man von Hämosiderose.
Als Hämochromatose wird in der Regel die idiopathische, genetisch bedingte Form einer vermehrten Eisenablagerung im Körper verstanden und nicht diejenige, die z. B. durch multiple Transfusionen zustande kommt.
Einteilung
- Idiopathische (genetische, primäre) Hämochromatose
- Erworbene (sekundäre) Hämochromatose (siehe unten)
Häufigkeit
Es handelt sich um eine der häufigsten Erbkrankheiten. Die Häufigkeit einer C282Y-Mutation liegt bei etwa 4 bis 9 % der Bevölkerung. Das Verhältnis manifest Erkrankter zu Gesunden liegt bei 1:500 bis 1:4000, das Verhältnis der Geschlechter m:f = 5:1 bis 10:1. Im Süden Europas kommt die familiäre Eisenspeicherkranheit weniger häufig vor als im Norden.
In Einer Studie an 50493 Blutspendern in Schweden wiesen 1,9 % eine Eisenüberladung auf. Von 840 mit Eisenüberladung waren 117 homozygot für C282Y und 97 zusammengesetzt heterozygot. 4
Eine weitere Studien besagt, dass etwa 1 von 10 männlichen HFE C282Y-Homozygoten im Laufe seines Lebens eine schwere Lebererkrankung entwickelt, wenn die Eisenüberladung nicht frühzeitig erkannt und behandelt wird. 5
Entstehung
Idiopathische Hämochromatose
Die Ursache der Eisenüberladung des Körpers ist eine Erhöhung der Eisenresorption im Dünndarm 6.
- Eine Mutation des HFE-Gens auf Chromosom 6 (C282Y-Mutation) ist die häufigste Ursache. HFE kodiert das Hämochromatoseprotein, das eine Rolle bei der Hepcidin-Regulation spielt.
- Seltene Ursachen (Nicht-HFE-Formen) betreffen
- eine mangelnde Aktivität von Transferrin Rezeptor 2 (TfR2),
- HAMP (hepcidin antimicrobial peptide, s. u.),
- Hemojuvelin (HJV, das Genprodukt des HFE2-Gens) oder
- Mutationen von Ferroportin.
Nicht-HFE-Formen der Eisenüberladung (aufgrund von Mutationen in HAMP, HJV oder TFR2) sind viel seltener als diejenige durch HFE-Mutationen. 7.
Die C282Y-Mutation im HFE-Gen ist bei Patienten keltischer Abstammung häufig zu finden. 8 Sie findet sich nicht oder selten bei Patienten nicht-keltischer Abstammung; dort ist von anderen Mutationen auszugehen. Die Mutationen H63D und S65C sind mit einer milderen Verlaufsform assoziiert.
→ Hepcidin
→ Eisenstoffwechsel
→ Entstehung der Hämochromatose
Erworbene Hämochromatosen
Erworbene Hämochromatoseformen beruhen auf einer sekundären Eisenüberladung des Körpers. Mögliche Ursachen einer Eisenüberladung sind folgende:
- häufige Transfusionen, z. B. bei der
- Porphyrie,
- Atransferrinämie,
oder der - Thalassämie.
- vermehrte Eisenzufuhr (z. B. durch in Eisenbehältern gebraute Getränke) 9
→ Eisenstoffwechsel
→ Entstehung der Eisenüberladung
Juvenile Hämochromatose
Die Hämochromatose Jugendlicher manifestiert sich meist zwischen dem 15. und 30. Lebensjahr und zeigt keine Assoziation mit dem HFE-Gen. Es besteht eine Assoziation mit homozygoten Genvarianten von HJV (Hämojuvelin) und anderen, wie HAMP. 10 Die Erkrankung ähnelt der HFE-Hämochromatose, verläuft aber schwerer.
Schon frühzeitig kommt es zu folgenden Störungen 11 12:
- Unterfunktion der Geschlechtsdrüsen (hypogonadotropischer Hypogonadismus),
- Herzmuskelerkrankung (Kardiomyopathie) mit lebensgefährlichen Rhythmusstörungen,
- Störung der Blutzuckerregulation (Glukoseintoleranz) und Diabetes,
- Gelenkstörungen (Arthropathie)
- Knochenabbau (Osteoporose),
- Vernarbung der Leber (Leberfibrose und Leberzirrhose).
Symptomatik
Die genetische HFE-Hämochromatose manifestiert sich bei Männern meist zwischen dem 30. und 50. Lebensjahr, bei Frauen wegen der Monatsblutungen, über die Eisen verloren geht, meist erst in der Menopause.
Leitsymptome:
- Hepatomegalie (Lebervergrößerung),
- Pigmentierung der Haut (bronzefarben- oder grau-bräunlich) in 50 % der Fälle,
- Diabetes mellitus (bei 20 % der Erkrankten im präzirrhotischen Stadium, bei 70 % der Erkrankten im Zirrhosestadium)
Weitere Symptome:
- Verlust der Körperbehaarung,
- Hodenatrophie, Libidoverlust,
- Splenomegalie (Milzvergrößerung),
- arthritische Gelenkbeschwerden,
- kardiale Symptome (häufig als erste Manifestation) mit Tachyarrhythmien bzw. Rechts-, Linksherzinsuffizienz (die Kardiomyopathie mit Herzrhythmusstörungen ist eine häufige Todesursache),
- Zeichen einer Leberzirrhose (häufig erste Manifestation),
- erhöhtes Risiko einer Peridontitis (Zahnfleischentzündung, abhängig von der Transferrinsättigung) 13.
Diagnostik
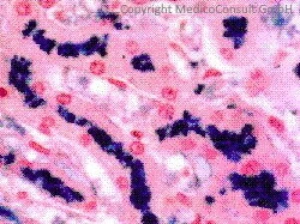
Anamnese und körperliche Befunde können erste Anhaltspunkte liefern, besonders wenn Kombinationen folgender Symptome und Befunde vorliegen: Leberzirrhose, Diabetes mellitus, pigmentierte Haut/Handlinien, Gelenkbeschwerden, Herzinsuffizienz und Herzrhythmusstörungen.
Die anschließende weitere Diagnostik durch Laborwerte und durch MRI T2 (eine Magnetresonanztomographie in T2-Wichtung) sichert die Diagnose. In den meisten Fällen kann auf eine Leberbiopsie verzichtet werden. 14
- Sicherung der Diagnose durch erhöhte Werte für Eisen i.S., Transferrinsättigung, Ferritin,
- die Transferrinsättigung und das Ferritin eignen sich zur Verlaufskontrolle unter Therapie,
- die genetische Untersuchung bzgl. Hämochromatose-Gen HFE-Mutation (relativ preiswert; dadurch erübrigt sich meist eine Punktion der Leber),
- die Bestimmung des Eisengehalts in der Leber kann durch CT oder MRT relativ sicher abgeschätzt werden. Die Magnetresonanztomographie eignet sich auch zur Verlaufskontrolle unter Therapie. 15
- Leberhistologie ist zur Diagnosestellung selten noch erforderlich, kann aber zur Stadieneinteilung sowie zur Verlaufs- und Prognosebeurteilung in Einzelfällen indiziert sein.
- Diagnostik von Komplikationen und Folgeschäden: dabei wird geachtet auf die Leber (Leberzirrhose, hepatozelluläres Karzinom?), die Hormondrüsen (Unterfunktionen?), das Herz (Herzrhythmusstörungen, Herzinsuffizienz?), die Gelenke (Schmerzen, Arthrose?)
→ Mehr zur Diagnostik siehe hier.
Komplikationen und Folgezustände
Die übermäßige und dauerhafte Speicherung von Eisen in den verschiedenen Organen und Geweben des Körpers hat vielfältige Folgen:
- Leberzirrhose,
- hepatozelluläres Karzinom: Die Hämochromatose ist eine Präkanzerose. Es besteht ein 200-fach erhöhtes Risiko für Leberkrebs (hepatozelluläres Karzinom, HCC); Alpha-Fetoprotein ist nur in einem Teil der Fälle positiv und damit ein schlechter Marker für das Hämochromatose-bedingte HCC 16,
- Herzinsuffizienz und Herzrhythmusstörung (häufige Todesursache),
- Diabetes mellitus (zusammen mit pigmentierter Haut: Bronzediabetes),
- Gelenkerkrankungen (Arthropathie), Differentialdiagnosen: rheumatoide Arthritis, degenerative Gelenkveränderungen (Arthrose),
- hormonelle Dysregulation verschiedener Hormondrüsen bis hin zur polyglandulären Insuffizienz: Die Hämochromatose wird als „endokrine Lebererkrankung“ aufgefasst 17.
Therapie
Folgende Punkte werden bei der Behandlung berücksichtigt:
- Die Therapie der Wahl zur Reduzierung der Eisenüberladung sind Aderlässe (z. B. wöchentlich 300 ml, bis die Eisenspeicher leer sind und der Hb-Wert zu sinken beginnt (Anämiebeginn). Der Erfolg wird über den Ferritinspiegel und eine Abnahme der Dichte im Computertomogramm kontrolliert.
- Unter der Aderlass-Therapie ist eine Besserung der Gelenksymptome nicht unbedingt zu erwarten.
- In besonderen Fällen kommt eine Behandlung mit Desferrioxamin (Eisenchelatbildner) in Betracht, die sehr viel weniger wirksam ist (Indikation z. B. bei der Thalassämie).
- Die orale Eisenaufnahme muss minimiert werden (u. a. kein Alkohol).
- In Endstadien der Leberzirrhose kommt eine Lebertransplantation in Betracht, die allerdings nicht zu einer Heilung führt, da das eigentliche Problem in einer unkontrollierten Eisenaufnahme im Darm liegt.
- Ansonsten bleiben nur symptomatische Maßnahmen als Therapiemaßnahmen.
- Ein Leberkrebs (hepatozelluläres Karzinom, HCC), der im Rahmen einer Hämochromatose gehäuft auftritt, wird je nach Größe und Ausbreitung sowie dem Stadium der Leberkrankheit (in zirrhotischer oder nicht zirrhotischer Leber) interventionell behandelt (siehe hier). Zu den Optionen gehören vor allem eine Resektion des Tumors, eine Radiofrequenzablation, eine lokale katheterbasierte Therapie („Verödung“) und eine Lebertransplantation. 18
→ Mehr zur Therapie siehe hier.
Prognose
Die 5-Jahres-Überlebensrate ohne Therapie beträgt 18%. Bei Therapiebeginn (Aderlässe) im präzirrhotischen Stadium resultiert eine praktisch normale Lebenserwartung. Bei Therapiebeginn erst im Zirrhosestadium ist die 5-Jahres-Überlebensrate 75 – 92 %, die 20-Jahres-Überlebensrate 46 – 49 %. Alkoholabusus und Leberentzündungen (Hepatitiden) verschlechtern die Prognose. 19
Vorbeugung
Die Vorbeugung von Langzeitfolgen einer Hämochromatose beruht im Wesentlichen auf einer frühen Erkennung.
- Screening: Wenn Blutuntersuchungen aus anderen Gründen anstehen, sollten mindestens einmal Eisen, Ferritin und ggf. die Transferrinsättigung bestimmt werden.
- Gezielte Untersuchung von Verwandten 1. Grades (Geschwister, Kinder).
- Bei bekannter Diagnose: absolute Alkoholkarenz, keine mit Eisen angereicherten Nahrungsmittel (z. B. manche Müsli), keine eisenhaltigen Präparate („Aufbaupräparate“, Präparate zur Blutbildung etc.).
Genetische Analyse (Bestimmung des HFE-Gens): Sie gehört zur Vorsorge hinzu, wenn bei nahen Blutsverwandten eine vermutlich genetisch bedingte Eisenüberladung diagnostiziert wurde. Wird eine Misch-Heterozygotie (C282Y/H63D) gefunden, so ist eine Eisenüberladung zwar nicht sehr wahrscheinlich, aber möglich (in einer Studie 5,3 % in 10 Jahren), so dass diese Genträger sowie auch deren Nachkommen in Kontrolle bleiben sollten. Es wird ein Bevölkerungsscreening auf HFE p.Cys282Tyr Homozygotie diskutiert 20.
Vorbeugende Aderlasstherapie: Bei Bestätigung einer genetischen Veranlagung zur hereditären Hämochromatose (Homozygotie des HFE-Gens) sollte vorbeugend schon vor einer klinischen Manifestationeine Aderlasstherapie in reduziertem Maße begonnen werden. Das gilt auch für die Erkennung einer Hämochromatose-Veranlagung bei Kindern und Jugendlichen. 21
→ Behandlung einer Hämochromatose
→ Auf facebook informieren wir Sie über Neues und Interessantes.
→ Verwalten Sie Ihre Laborwerte mit der Labor-App Blutwerte PRO – mit Lexikonfunktion.
Verweise
- Hämochromatose Entstehung
- Hämochromatose Diagnostik
- Hämochromatose Therapie
- Eisenstoffwechsel
- Hämochromatose – einfach erklärt
- Die Leber
Referenzen
- Nat Rev Dis Primers. 2018 Apr 5;4:18016. doi: 10.1038/nrdp.2018.16.[↩]
- Transl Gastroenterol Hepatol. 2020 Apr 5;5:25. doi: 10.21037/tgh.2019.11.15. [↩]
- Am Fam Physician. 2021 Sep 1;104(3):263-270. [↩]
- Ann Hematol. 2020 Oct;99(10):2295-2301. DOI: 10.1007/s00277-020-04146-8[↩]
- Genet Med. 2018 Apr;20(4):383-389. DOI: 10.1038/gim.2017.121[↩]
- Nat Rev Dis Primers. 2018 Apr 5;4:18016. doi: 10.1038/nrdp.2018.16[↩]
- Nat Rev Dis Primers. 2018 Apr 5;4:18016. doi: 10.1038/nrdp.2018.16[↩]
- Nat Genet 1996; 13: 399-408; Blood Cells Mol Dis 1996; 22: 187-194[↩]
- Liver Cancer. 2014 Mar;3(1):31-40.[↩]
- Blood Cells Mol Dis. 2019 Feb;74:30-33. doi: 10.1016/j.bcmd.2018.10.006. [↩]
- Eur J Hum Genet 1997; 5: 371-375[↩]
- Juvenile Hemochromatosis. 2005 Feb 17 [updated 2020 Jan 9]. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Stephens K, Amemiya A, editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993–2020. PMID: 20301349.[↩]
- Sci Rep. 2018 Oct 19;8(1):15532. doi: 10.1038/s41598-018-33813-0.[↩]
- Am J Gastroenterol. 2019 Aug;114(8):1202-1218. DOI: 10.14309/ajg.0000000000000315.[↩]
- Magn Reson Imaging. 2005; 23: 1-25[↩]
- Pathol Oncol Res. 2020 Apr;26(2):599-603. doi: 10.1007/s12253-019-00585-5[↩]
- Hepatology. 2007 Oct;46(4):1291-301. doi: 10.1002/hep.21886[↩]
- Am J Clin Oncol. 2019 Dec;42(12):918-923. doi: 10.1097/COC.0000000000000583.[↩]
- Gastroenterology 1996; 110: 1107-1119[↩]
- JAMA Netw Open. 2023 Oct 2;6(10):e2338995. doi: 10.1001/jamanetworkopen.2023.38995[↩]
- Juvenile Hemochromatosis. 2005 Feb 17 [updated 2020 Jan 9]. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Stephens K, Amemiya A, editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993–2020. PMID: 20301349.[↩]