Das Wichtigste
Die Porphyria cutanea tarda (PCT), früher auch als chronische hepatische Porphyrie bezeichnet, ist die häufigste Porphyrieform beim Menschen. Sie ist eine photoreaktive Hauterkrankung, die durch die Hemmung oder einen genetischen Defekt des Häm-Biosynthese-Enzyms Uroporphyrinogen-Decarboxylase (UROD) in der Leber verursacht wird. Zwei Hauptformen werden unterschieden: eine sporadische Form (Typ-I-PCT) und eine familiäre Form (Typ-II-PCT). Beide haben eine verminderte UROD-Aktivität in der Leber zur Voraussetzung, beide werden auch durch Umweltfaktoren getriggert. Die PCT ist charakterisiert durch bullöse Hautläsionen und eine massive Ausscheidung von Uroporphyrin mit dem Urin (Rotfluoreszenz im uv-Licht). Eine Leberschädigung kommt vor, ist aber unterschiedlich ausgeprägt. Ihr Ausmaß ist abhängig von zusätzlichen pathogenetischen Faktoren, zu denen Alkohol, Rauchen, Östrogene und das Hämochromatose-Gen gehören. Zur Behandlung gehören vor allem eine strikte Vermeidung kritischer Faktoren wie Alkohol, Rauchen, Östrogenen und auslösenden Medikamenten sowie eine Entfernung von Eisen bei einer Eisenüberladung durch Aderlässe. Ein wirksames Medikament zur Langzeitprophylaxe und Akuttherapie ist Hydroxychloroquin. |
Häufigkeit
Die Porphyria cutanea tarda (PCT) ist unter den seltenen Stoffwechselkrankheiten relativ häufig; die Inzidenz liegt bei 1 auf 10000. Das Hauptmanifestationsalter liegt jenseits von 50 Jahren. Männer sind geringfügig häufiger betroffen als Frauen.
Entstehung
Sowohl genetische als auch Umweltfaktoren spielen bei der Entwicklung einer symptomatischen Porphyria cutanea tarda zusammen.
Porphyrine sind Zwischenprodukte in der Synthese von Häm, einem eisenhaltigen Molekül, das für die Funktion des Hämoglobins und vieler Cytochrome erforderlich ist. Die Aktivität der Uroporphyrinogen-Decarboxylase (UROD), des 5. Enzyms in der Hämsynthese, ist bei der PCT auf unter 20% vermindert. Dieses Enzym katalysiert die Umwandlung von Uroporphyrinogen zu Coproporphyrinogen. Inzwischen sind mindestens 13 Mutationen der UROD bekannt.
Im Zytosol von Leberzellen wurde ein UROD-Inhibitor gefunden, der bei der Pathogenese der PCT eine Rolle spielt. 1
Durch die Abnahme der Enzymaktivität sammelt sich Uroporphyrin (das Oxidationsprodukt von Uroporphyrinogen) in der Leber an und gelangt über die Blutbahn zur Haut. 2 3
Reaktionen in der Haut
Uroporphyrin der Haut wird durch langwelliges uv-Licht aktiviert; es entstehen reaktive Sauerstoffspezies, die an den belichteten Arealen zu einer oxidativen Schädigung mit bullösen Hautveränderungen (Blasenbildungen) führen.
Reaktionen in der Leber
Uroporphyrinogen, das Substrat der UROD, wird zu Uroporphyrin oxidiert und sammelt sich in der Leber an. Es führt zu einer Leberzellschädigung, deren Ausprägung sehr unterschiedlich sein kann. Wenn individuelle Faktoren, die die Reaktionsbereitschaft der Leber erhöhen, hinzukommen, kann es zu schweren Leberschäden kommen.
Faktoren, welche die Leberempfindlichkeit erhöhen
Faktoren, die für eine akute Symptomatik empfänglich machen, (Suszeptibilitätsfaktoren) sind einer Studie zufolge Alkoholgenuss (87 %), Rauchen (81 %), chronische Hepatitis C (69 %) und Mutation des HFE-Gens (53 %). 4
Eisengehalt der Leber: Bei den meisten Patienten mit PCT lässt sich in der Leberhistologie eine Siderose (Eisenanhäufung) feststellen. Alkoholkonsum, eine chronische Hepatitis C und das HFE-Gen senken die Aktivität von Hepcidin, erhöhen die Eisenresorption im Darm und steigern den Eisengehalt der Leber. 5 Eisen ist neben CYP1A2 (s. u.) ein essenzieller Faktor in der Pathogenese der PTC: in Mäusen mit Eisenmangel entwickelt sich eine Porphyrie unter Induktionsbedingungen nicht. 6 Eine der PTC-induzierenden Funktionen des Eisens scheint darin zu bestehen, dass es die Oxidation von Uroporphyrinogen zu Uroporphomethen fördert, was UROD kompetitiv hemmt. 7 Die PTC-Erkrankung lässt sich durch eine Eisenentlastung bessern (s. u.).
Oxidativer Stress der Hepatozyten (Leberzellen): Alkokol, Hepatitis C und Östrogene erhöhen die Produktion reaktiver Sauerstoffspezies in den Zellen.
Cytochrom 1A2: Rauchen und Alkohol induzieren Cytochrom-P450-Enzyme, so auch CYP1A2. Dieses Cytochrom ist wesentlich für die Entstehung einer Uroporphyrie im Mausmodell; seine Abwesenheit (in Knock-out-Mäusen) schützt vor der lebertoxischen Wirkung des Uroporphyrins. 8 Bei PTC-Patienten wurden zwei Allele identifiziert (CYP1A2*1F und GSTM1, g-163A), die mit der Entwicklung einer PTC assoziiert sind. 9 In einer französischen Studie spielte der CYP1A2-Genotyp jedoch keine Rolle bei PCT-Patienten. 10
Antikörper gegen ein zytosolisches Leberprotein (40000 kDa) werden gehäuft bei der Hepatitis-C-assoziierten PCT gefunden. 11
Formen der PTC
Die sporadische bzw. erworbene Form (Typ I) wird durch Alkohol, Rauchen, Hepatitis C, HIV, Lupus erythematodes, Östrogene, Medikamente und verschiedene Chemikalien ausgelöst. 2 12
Die hereditäre Form (Typ II) ist durch das Auftreten von PCT-Fällen in der Familie gekennzeichnet; oft lässt sich lediglich eine erhöhte Sonnenempfindlichkeit in der Familienanamnese eruieren. Es sind inzwischen eine Reihe von Genen bekannt, deren Mutation diese Form auslösen. ((Mol Genet Metab. 2018 Nov 28. pii: S1096-7192(18)30642-5. doi: 10.1016/j.ymgme.2018.11.013.)
Tritt die PCT in der Familien sporadisch auf, wird sie als Typ III bezeichnet. Wenn (selten) ein homozygoter UROD-Defekt vorliegt, wird sie als Typ IV bezeichnet wird und führt bereits in der Kindheit zu Symptomen.
Symptomatik
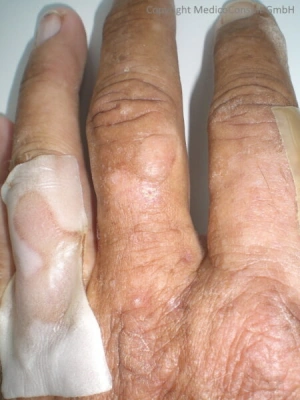
Hautmanifestationen: Die Symptomatik der Porphyria cutanea tarda wird durch die bullösen Hautläsionen an sonnenexponierten Stellen des Körpers bestimmt. Oft lässt sich eine vermehrte Behaarung des Körpers und des Gesichts erkennen. Die Haut ist oft vermehrt vulnerabel und elastisch. Bei beiden PCT-Typen (I und II) hängen die Hauterscheinungen von zusätzlichen Faktoren ab, die die UROD zusätzlich in ihrer Aktivität hemmen. 13
Lebersymptome: Klinische Zeichen einer chronischen Lebererkrankung mit Cholestase und Entwicklung einer Leberzirrhose treten nur sporadisch auf.
Diagnostik
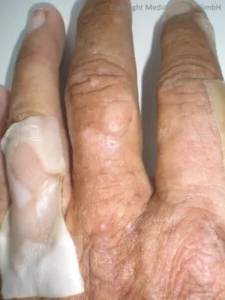
Die Diagnose einer Porphyria cutanea tarda gerät durch die typischen bullösen Hautläsionen (Blasenbildungen), die Abheilungsnarben an lichtexponierten Stellen des Körpers und Hyperpigmentationen ins Blickfeld. Auch andere Porphyrie-Typen verursachen solche Hautläsionen, so auch die hereditäre Koproporphyrie und die Porphyria varegata. Diese Typen weisen jedoch im Urin einhöhte Werte für Delta-Aminolävolinsäure und Prophobilinogen auf, was bei der PCT nicht der Fall ist.
UROD- und HFE-Genanalyse können zur Diagnostik beitragen. Eine Mutation in diesen Genen ist jedoch nicht Voraussetzung für die Diagnose. In einem großen Teil der Fälle liegt eine Hemmung der normalen (genetisch nicht mutierten) UROD vor.
Laborbefunde
Marker des Eisenstoffwechsels (Eisen, Ferritin und Transferrin-Sättigung) sind deutlich erhöht, Leberwerte können erhöht sein. Im Urin der PCT dagegen finden sich große Mengen an Uroporphyrin (unter der uv-Lampe rot fluoreszierend), jedoch kein Porphobilinogen und D-ALA.
Therapie
Grundlage jeder PCT-Therapie ist die strikte Vermeidung auslösender Faktoren wie Alkohol, Rauchen, Östrogenen und auslösenden Medikamenten.
→ Liste unsicherer und sicherer Medikamente
Aderlass-Therapie
Am besten wirken wiederholte Aderlässe zur Entfernung vermehrten Körpereisens bis zur Anämiegrenze. 5 2
Hydroxychloroquin
Eine Hydroxychloroquin-Therapie in niedriger Dosierung ist laut einer Studie an 48 unselektierten Patienten bei der Behandlung von Patienten mit Porphyria cutanea tarda ebenso wirksam wie eine Aderlassbehandlung 14. Eine chinesische Arbeit weist nach, dass eine kurzzeitige orale Hochdosis-Behandlung mit Hydroxychloroquin bei Patienten mit PCT zu einer raschen Remission führen kann. 15 Eine Therapie der Hepatitis C vermag einen PCT-Schub auszulösen. Sie können mit Hydroxychloroquin effektiv behandelt werden. Die neuen DAA’s führen laut einer Zusammenstellung nicht zu einer Schubauslösung. 16
Bei Niereninsuffizienz- und Dialyse-assoziierter PCT ist Chloroquin wirkungslos. Kleine wiederholte Aderlässe unter Erythropoetin-Gabe oder Desferrioxamin werden empfohlen. 17
Risiken und Prognose
Die PCT bedeutet für die Betroffenen ein erhöhtes Risiko für Leberkrebs (HCC, etwa 20-fach), Gallenwegskrebs (cholangioläres Karzinom, CCC) und Gallenblasenkrebs (etwa 7-fach) sowie für einen vorzeitigen Tod (1,5-fach). Ein Teil des Risikos mag einem ungesunden Lebensstil zuzuschreiben sein (vor allem Alkoholabusus und Rauchen), ein Teil wird aber auch der Grunderkrankung zugeordnet. 18
Es besteht ein deutlich erhöhtes Risiko für eine frühzeitige Berentung. Oft steht sie im Zusammenhang mit Komorbiditäten wie bösartigen Neubildungen, Alkoholabhängigkeit, neurotischen und affektiven Störungen, sowie mit Erkrankungen des Bewegungsapparats und des Bindegewebes 19.
→ facebook: Neues und Interessantes!
→ Labor-App Blutwerte PRO – mit Lexikonfunktion
Verweise
Weiteres
- Blood Cells Mol Dis. 2011 Dec 15;47(4):249-54. doi: 10.1016/j.bcmd.2011.07.006[↩]
- Mol Genet Metab. 2019 Jan 18. pii: S1096-7192(18)30579-1. doi: 10.1016/j.ymgme.2019.01.004.[↩][↩][↩]
- Best Pract Res Clin Gastroenterol. 2010 Oct;24(5):735-45. doi: 10.1016/j.bpg.2010.07.002.[↩]
- Clin Gastroenterol Hepatol. 2010 March; 8(3): 297–302.e1[↩]
- Liver Int. 2012 Jul;32(6):880-93[↩][↩]
- Biometals. 2009 Apr;22(2):345-51[↩]
- Proc Natl Acad Sci U S A. 2007 March 20; 104(12): 5079–5084[↩]
- Toxicol Appl Pharmacol. 2001 Jun 1;173(2):89-98[↩]
- Mol Med. 2011 Mar-Apr; 17(3-4): 241–247[↩]
- Br J Dermatol. 2012 Feb;166(2):425-9. doi: 10.1111/j.1365-2133.2011.10642.x[↩]
- Clin Exp Immunol. 2001 October; 126(1): 47–53[↩]
- Am J Case Rep. 2014 Jan 21;15:35-40. doi: 10.12659/AJCR.889955. eCollection 2014.[↩]
- Mol Genet Metab. 2018 Nov 28. pii: S1096-7192(18)30642-5. doi: 10.1016/j.ymgme.2018.11.013.[↩]
- Clin Gastroenterol Hepatol. 2012 Dec;10(12):1402-9. doi: 10.1016/j.cgh.2012.08.038[↩]
- AME Case Rep. 2022 Apr 25;6:19. doi: 10.21037/acr-21-77[↩]
- Am J Med Sci. 2017 Jun;353(6):523-528. doi: 10.1016/j.amjms.2017.03.007.[↩]
- Expert Opin Pharmacother. 2005 Mar;6(3):377-83[↩]
- Orphanet J Rare Dis. 2019 Apr 3;14(1):77. doi: 10.1186/s13023-019-1051-3.[↩]
- Orphanet J Rare Dis. 2022 Feb 22;17(1):72. doi: 10.1186/s13023-022-02201-3. Erratum in: Orphanet J Rare Dis. 2022 May 4;17(1):180. doi: 10.1186/s13023-022-02329-2.[↩]
- Hematology Am Soc Hematol Educ Program. 2024 Dec 6;2024(1):450-456. doi: 10.1182/hematology.2024000664[↩]
- Rudnick S, Phillips J, Bonkovsky H; Porphyrias Consortium of the Rare Diseases Clinical Research Network. Familial Porphyria Cutanea Tarda. 2013 Jun 6 [updated 2022 Jun 9]. In: Adam MP, Bick S, Mirzaa GM, Pagon RA, Wallace SE, Amemiya A, editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993–2026. PMID: 23741761.[↩]
- Cureus. 2025 Jul 15;17(7):e87965. doi: 10.7759/cureus.87965[↩]