Eine Polycythämia vera liegt vor, wenn die Bildung der Blutzellen im Knochenmark auf genetischer Basis unkontrolliert und übermäßig abläuft. Sie gehört zu den myeloproliferativen Erkrankungen. Sie ist von sekundären Formen einer Polyzythämie und einer Polyglobulie abzugrenzen.
Entstehung der PV
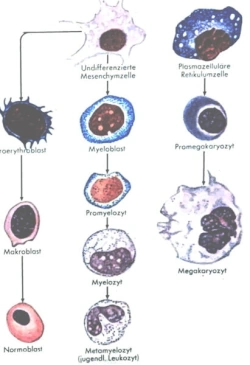
An der Entstehung einer Polycythaemia vera ist die Tyrosinkinase JAK2 beteiligt. Sie reguliert die Zellproliferation im Knochenmark über Erythropoetin. Die Mutation JAK2 V617F führt zu inadäquater unregulierter Stimulation der Stammzellen im Knochenmark. Die Rezeptoren für die Stimulatoren Erythropoetin, Thrombopoetin und Granulozyten-stimulierenden Faktor (GCSF) sind aktiviert, was erklärt, dass alle drei Zellreihen des Knochenmarks proliferieren. Die unkontrollierte Blutbildung beschränkt sich nicht nur auf das Knochenmark, sondern expandiert auf die Milz, die sich dadurch vergrößert, und später auch auf die Leber. Es kann zu einer tastbaren Vergrößerung der beiden Organe, einer Hepatosplenomegalie, kommen. 1 2
Klinik der PV
Die jährliche Inzidenz beträgt in den USA 0,5 bis 4,0 Fälle pro 100.000 Personen 3. Die Prävalenz liegt bei etwa 1 Fall auf 100 000; der Altersgipfel liegt bei 60 bis 70 J, das Verhältnis Männer zu Frauen bei 2:1.
Typisch für Polycythaemia vera sind folgende Befunde:
- Eine Milzvergrößerung (Splenomegalie) kann tastbar werden. Auch eine Vergrößerung Leber (Hepatosplenomegalie) kann sich entwickeln. Bei einer starken Vergrößerung der Organe steigt die Gefahr einer Organruptur und intraperitonealen Blutungen (in den Bauchraum).
- Im peripheren Blut erhöht sich der Hämatokrit; die Fließeigenschaft des Bluts nimmt ab; die Gefahr von Thrombosen, Lungenembolien, einem Herzinfarkt und einem Schlaganfall steigt. Wiederholte Schlaganfälle können auf eine Polyzythämie zurückzuführen sein. 4
- Chronische Geschwüre (Ulzerationen) treten auf; sie sind durch die schlechte Fließeigenschaft des Bluts bedingt. 5
- Durch die Minderwertigkeit der übermäßig produzierten Thrombozyten (Thrombopathie) kann auch eine paradoxe Blutungsneigung eintreten.
- Das Gesamtvolumen des Bluts steigt und damit oft auch der Blutdruck.
- Der erhöhte Zellumsatz führt zu einer erhöhten Harnsäurebildung (Abbauprodukt der DNA) mit dem Risiko von Gichtanfällen.
Symptome und Diagnostik
Die Symptomatik ist eher unspezifisch und besteht aus Müdigkeit, Nachtschweißen und Juckreiz, zudem kommen häufig .Juckreiz (Pruritus, 33 %), vorübergehende Sehstörungen (14 %) vor. Klinisch kann eine tastbare Milzvergrößerung (Splenomegalie, 36 %) auffallen. 6
Laborwerte: Die Polycythaemia vera gerät in der Regel zufällig ins Blickfeld, wenn im Rahmen einer Abklärung der Symptomatik ein zunächst nicht erklärbar erhöhter Hämatokrit und eine Thrombozytose gefunden werden. Es besteht eine Erythrozytose (Hämoglobin >16,5 mg/dl bei Männern oder >16,0 mg/dl bei Frauen). Häufig sind eine Thrombozytose (53 %) und Leukozytose (49 %) zu finden. Die Diagnostik umfasst ein Differenzialblutbild und eine Knochenmarkpunktion. Im Knochenmark wird eine vermehrte Proliferation aller drei Stammzellreihen gefunden.
Molekulargenetische Untersuchung: Die für die Polycythämie verantwortliche JAK2(V617F)-Mutation ist bereits in sehr frühen Stadien nachweisbar.
Therapie
Die Therapie der Polyzythämia vera umfasst folgende Maßnahmen:
- Aderlässe (Phlebotomie) gegen die Polyglobulie und
- Chemotherapie mit Hydroxyharnstoff (Litalir) zur Senkung der Leukozyten- und Thrombozytenzahl.
- Ruxolitinib (ein Januskinase-Inhibitor, Jakafi ®): Es kommt bei mangelhaftem Ansprechen auf Hydroxyurea in Betracht. 7 Ruxolitinib wurde in einer Studie gut vertragen und war der besten verfügbaren Therapie (einschließlich Interferon [IFN]) bezüglich Hämatokrit und Normalisierung des Blutbildes sowie der Symptomatik überlegen. 8 Die Zahl der Aderlässe ließ sich durch das Medikament in einer real-world-Studie bedeutend reduzieren. 9 In den ersten 10 Jahren nach Zulassung hat sich Ruxolitinib zu einer sicheren und wirksamen Standardtherapie für die PV entwickelt 10.
Verweise
Weiteres
- Blood. 2023 Apr 20;141(16):1934-1942. doi: 10.1182/blood.2022017697[↩]
- Ann Intern Med. 2010 Mar 2;152(5):300-6. doi: 10.7326/0003-4819-152-5-201003020-00008.[↩]
- JAMA. 2025 Jan 14;333(2):153-160. doi: 10.1001/jama.2024.20377[↩]
- BMJ Case Rep. 2015 Mar 9;2015. pii: bcr2014207625. doi: 10.1136/bcr-2014-207625.[↩]
- J Foot Ankle Surg. 2013 Nov-Dec;52(6):781-5[↩]
- Blood. 2014 Jun 12; 123(24):3803-10.[↩]
- N Engl J Med. 2015 Jan 29;372(5):426-35. doi: 10.1056/NEJMoa1409002.[↩]
- Ann Hematol. 2018 Apr;97(4):617-627. doi: 10.1007/s00277-017-3225-1[↩]
- Clin Lymphoma Myeloma Leuk. 2020 Oct;20(10):697-703.e1. DOI: 10.1016/j.clml.2020.05.019[↩]
- Cancer. 2025 Jan 1;131(1):e35661. doi: 10.1002/cncr.35661[↩]